קרן של תקווה
קבוצת המחקר של עמית מלר מהטכניון זכתה במענק מיוחד מהאיחוד האירופי שנועד להאיץ טכנולוגיה חדשנית לקידוח חרירים ננו-מטריים בחומר באמצעות קרן לייזר. ההתקן הסופי ישמש לאנליזה של מולקולה בודדת לטובת אבחון מהיר של מחלות ובהן COVID-19
קבוצת המחקר של פרופ’ עמית מלר מהפקולטה להנדסה ביו-רפואית בטכניון זכתה במענק ERC PoC – מענק להוכחת היתכנות, בסך של 150 אלף יורו. המענק המיוחד מהנציבות האירופית למחקר הוענק לאחרונה ל-55 חוקרים, והוא נועד לסייע להם למצות את פוטנציאל המסחור של פיתוחיהם. הפרויקט של פרופ’ מלר נקרא OptiPore ומטרתו לקדם טכנולוגיה חדשנית לאנליזה של מולקולות בודדות בכלל ולזיהוי נוכחות של נגיף הקורונה SARS-CoV-2 בפרט. האמצעי: פיתוח שיטה חדשנית מהירה וזולה ליצירת ssNPs – התקני אבחון המבוססים על חרירים ננומטריים.
ssNPs היא משפחה חדשה של התקנים שמטרתם אנליזה של מולקולות ביולוגיות בודדות. לאנליזה כזאת יש ערך רפואי ומחקרי עצום, שכן היא מחליפה שיטות אבחון קיימות המבוססות על אנליזה של תמיסה שלמה – שיטות המאופיינות בחסרונות רבים ובהם עלות גבוהה, ציוד מסורבל ודיוק מוגבל.
כדי להמחיש את קפיצת המדרגה הטמונה בהתקני ssNPs ניקח לדוגמה את נגיף הקורונה SARS-CoV-2. בדיקות הקורונה הקיימות מבוססות על טכנולוגיית RT-qPCR, המצריכה תהליך ארוך ומורכב הכולל את איסוף הדגימה מהנבדק באמצעות מטוש, “פתיחה” של הנגיף כדי לחשוף את החומר הגנטי שבתוכו, מיצוי החומר הגנטי של ה-RNA, ו”שיעתוק לאחור” שבו מתורגמים רצפי ה-RNA לרצפי DNA. אולם בכך לא תם התהליך, שכן כדי שהמכשור הקיים יוכל לזהות נוכחות נגיפים בדגימה מבוצעת בשלב זה הגברה מעריכית (PCR) המכפילה שוב ושוב את מולקולות ה-DNA כדי לייצר מסה קריטית שלהן. מלבד היותו של התהליך ארוך ויקר, שלב ההגברה יוצר במקרים מסוימים טעויות משמעותיות בקביעת נוכחות הנגיף, כלומר בהכרעה אם הנבדק מאומת או שלילי לקורונה.
תהליך האבחון שפיתחה קבוצת המחקר של פרופ’ מלר מייתר לחלוטין את שלב ההגברה המעריכית ומאפשר ספירה וכימות ישירים של מולקולות הנגיף. כך נחסך זמן יקר ונמנעות אותן טעויות. השיטה החדשה מבוססת על משיכת מולקולות ביולוגיות בודדות כגון די-אן-איי, אר-אן-איי או חלבונים, באמצעות שדה חשמלי, לתוך “חריר ננומטרי” המכיל חיישנים חשמליים או אופטיים. הפלט האלקטרוני עובר ניתוח חישובי המאפשר זיהוי וספירה ישירה ומיידית של המולקולות.
זמן קצר לאחר פרוץ מגפת הקורונה החל פרופ’ מלר לעבוד על התאמה של טכנולוגיה זו לצורך הדחוף בבדיקות קורונה מהירות ומדויקות. ואכן, בהוכחת ההיתכנות הודגמה יעילותה של שיטה זו בניטור נוכחות SARS-CoV-2 גם כאשר הדגימה המקורית מכילה כמות זעירה של נגיפים. תהליך זה, שפורסם לאחרונה ב-ACS Nano, פותח על ידי פרופ’ מלר וצוות המחקר עם הפוסט-דוקטורנטית ד”ר יאנה רוזבסקי ועמיתיהם בבית החולים “שריטה” בברלין, וזאת בסיוע מענק ERC שהקצה האיחוד האירופי כדי להאיץ את מסחור הבדיקה.
כעת, כאמור, זכתה הקבוצה במענק ERC משלים. מענק זה אינו מתמקד בפיתוח הבדיקה עצמה אלא בתהליך הייצור של ההתקן, שכן קדיחת החרירים היא אתגר טכנולוגי עצום המעכב כיום את פיתוחם הנרחב של התקני ssNPs. בעבודה ממושכת ומעמיקה פיתחה קבוצת המחקר של פרופ’ מלר טכנולוגיה ייחודית לקדיחת החרירים בהתקני האבחון, וזאת באמצעות קרן לייזר כחולה ממוקדת. טכנולוגיה זו תפותח כעת, בסיועו של המענק, כדי להביא אותה לשימוש קליני בהקדם האפשרי.
ראוי לציין כי אף ששני המענקים הוקצו בשעה שהעולם מתמודד עם מגפת הקורונה, הטכנולוגיות האמורות רלוונטיות לאבחון מחלות רבות – לא רק מחלות נגיפיות וחיידקיות אלא גם סוגי סרטן שונים, כפי שכבר הודגם בצורה ראשונית במעבדת הטכניון. מחקר הקורונה נעשה בשיתוף פעולה עם יחידת הביו-בנק במרכז הרפואי רמב”ם.
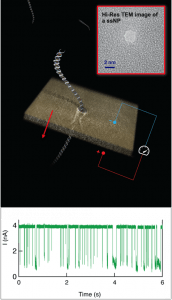
- באיור: העברת הדגימה בחריר הנומטרי המיוצר בשכבת סיליקון ניטריד דקיקה – ואנליזה של הדגימה. הגרף התחתון מציג את מדידת הזרם החשמלי בחריר – כך נספרות מולקולות הנגיף.
- משמאל: מדידת הזרם בננו-חריר מאפשרת ספירה ישירה של מולקולות הנגיף (מסומנות בכוכביות אדומות) בהשוואה למולקולות די-אן-איי רגילות. באמצע: האותות החשמליים עוברים עיבוד ממוחשב בתוכנה המבוססת על למידת מכונה. מימין: השלבים הקודמים מפיקים כימות מדויק של הביטוי של גן הבקרה האנושי והגן הנגיפי. מתוך היחס ביניהם אפשר לכמת את חומרת ההידבקות בנגיף SARS-CoV 2